
—истема химических обозначений, созданна€ ∆ераром
»так, с началом крушени€ дуалистической системы возник вопрос о новых критери€х классификации органических соединений. ’имическа€ практика требовала, чтобы классификаци€ исходила из химических свойств соединений и генетических св€зей, опиралась на единые химические формулы, которые выводились бы из объективных эмпирических данных, а не из гипотез о внутренних группировках атомов. »менно в такой обстановке рождаетс€ система ∆ерара Ч попытка создать естественную и рациональную классификацию органических веществ.
”же в первых работах ∆ерара про€вл€етс€ его склонность к обобщени€м и систематизации эмпирического материала. “ак, в 1835 г. он подвергает пересмотру формулы природных силикатов [2] и предлагает свою классификацию этих соединений. Ёта работа восемнадцатилетнего ∆ерара получила положительную оценку маститого Ѕерцелиуса: Ђ∆ерар проделал весьма похвальную работу, пересчитав результаты анализов большого числа природных силикатов, чтоб сравнить с прин€тыми дл€ них формулами. ќн обнаружил, таким образом, много ошибок, более или менее значительных, которые €вл€лись или ошибками расчета, или опечатками, переписанными различными авторами друг у друга. роме этой кропотливой и полезной работы, он еще способствовал установлению новых формулї [3, стр. 165].
¬ начале своей педагогической де€тельности ∆ерар невольно был вынужден обратить внимание на отсутствие единой классификации органических веществ. »сход€ из опытных данных о разложени€х и превращени€х органических веществ, он приходит к важным теоретическим выводам о химических формулах органических соединений и о системе атомных весов. Ђя доказываю, Ч пишет молодой ученый, Ч что химик делает противоположное тому, что делает жива€ природа: он сжигает, разрушает, действует методом анализа. “олько жизненна€ сила действует методом синтеза, она восстанавливает здание, разрушенное химическими силами. ќтсюда следует, что хороша€ классификаци€ может быть создана на основе продуктов разложени€ веществї [33, стр. 498]. ƒалее ∆ерар указывает, что при окислении или разложении органических веществ всегда выдел€ютс€ угольна€ кислота C4O4 и вода H4O2, а при разложении азотистых соединений Ч еще и аммиак N2H6 («нак Az, прин€тый во ‘ранции дл€ азота, мы везде заменили международным знаком N). «десь ∆ерар пользуетс€ удвоенными формулами, принима€ — = 6 (система ƒюма). “ак, разложение бензойной кислоты он изображает
C28Hl2O4 = C4O4 + C24Hl2.
¬ системе Ћибиха и Ѕерцелиуса, где — = 12, эта реакци€ выражалась иначе.
C14H12O4 = C2O4 + Cl2Hl2
(а в современных формулах эта же реакци€ выгл€дит так: —7Ќ6O2 = —O2 + —6Ќ6).
∆ерар замечает, что молекул€рный объем C4O4, H4O2 и N2H6 в газообразном состо€нии равен четырем. ѕоскольку угольна€ кислота и вода имеют такой же объем, как и всеми признанный эквивалент аммиака, значит их истинными эквивалентами будут —4O4 (¬ системе ƒюма двуокись углерода обозначалась —2O2, а окись углерода - —2O (— - 6,0 - 16)) и H4O2. ќтсюда он делает вывод, что пон€ти€ Ђэквивалентї и Ђобъемї тождественны. »сход€ из этого, ∆ерар отвергает формулу Ќќ дл€ воды, которую принимали сторонники системы эквивалентов (формула H4ќ2 соответствовала 2Ќ2O в системе Ѕерцелиуса), и считает, что эквивалент (молекула) воды состоит из одного эквивалента (O2) кислорода и двух эквивалентов (O2) водорода, ибо если O2 соответствует одному объему, то H4 соответствует двум объемам. ќн пишет: Ђ¬ода содержит 2 эквивалента, или атома, или объема, водорода и 1 эквивалент, или атом, или объем кислорода; ее формула должна быть Ќ2O (Ќ = 12,5, O = 200)ї [9, т. I, стр. 313]. “аким образом, ∆ерар, хот€ и смешива€ пон€ти€ атома и эквивалента, возвращаетс€ к формуле воды H2O, впервые предложенной јвогадро и примен€вшейс€ к системе Ѕерцелиуса 1826 г.
ѕо мнению ∆ерара, во всех химических формулах имеетс€ только четное число атомов кислорода. роме этого, при разложении органического вещества никогда не выдел€етс€ —2O2, —6ќ6 или —10ќ10, а всегда —4O4 (в современных формулах 2—ќ2 или 2n—O2) или кратное ему количество. ЂЌе только эквивалент угольной кислоты будет —4O4 и, следовательно, окись углерода —4O2, но по этим же соображени€м эквивалент углерода будет —4 = 150, если прин€ть O = 100. Ќо мы сейчас увидим, ч,то согласно нашему обозначению эквивалент кислорода будет O2 = 200, эквивалент водорода = 12,5; так что формулы —4O4 и —4O2 будут изображатьс€ в эквивалентах таким образом: окись углерода —ќ = 350; угольна€ кислота —O2 = 550; Ќ = 12,5ї (≈сли вместо Ќ = 12,5 вз€ть Ќ = 1, то получитс€, что ќ = 16, — - 12, —ќ = = 28, —02 - 44). ∆ерар считает, что его новые формулы подтверждают правильность водородной теории кислот: Ђ≈сли в действительности эквивалент воды Ќ4O2<...> то конституци€ солей, прин€та€ всеми химиками, не может быть признанной, ибо тогда, например, свободна€ уксусна€ кислота уже никак не может быть ацетатом воды —8Ќ3ќ3ХЌ2O (— = 6), так как Ќ2O будет только половиной эквивалента воды. ¬ этом отношении только теори€ типов находитс€ в соответствии с опытомї [9, т. I, стр. 314]. Ётот вывод привел ∆ерара к необходимости изменить атомные веса металлов. “ак, исход€ из своих правил, он пишет реакции образовани€ уксуснокислого и сернокислого свинца следующим образом:
2—8Ќ8O4 + –b2ќ2 = 2—8(Ќ6–№)O4 + Ќ4O2
S2H4O8 + –b2O2 = S2–b2O8 + Ќ4O2
‘ормула R2O2 дл€ окислов металлов при ќ = 100 становитс€ R2O при ќ = 200. »сход€ из этого, ∆ерар считает нужным и Ђэквивалентыї металлов уменьшить вдвое по сравнению со значени€ми, которые они имели в системе эквивалентов или в системе Ѕерцелиуса. ƒело в том, что обе эти системы исходили из формулы RO дл€ низших окислов металлов.
ѕоскольку все химические формулы должны соответствовать тому же объему, что и —4O4 и Ќ4O2 (т. е. четырем объемам, если прин€ть, что объем одного атома Ќ равен 1), ∆ерар предлагает исправить те формулы органических соединений, которые отклон€лись из этого правила: например, удвоить формулы щавелевой кислоты и этилового эфира, соответствовавшие двум объемам.
“аким образом, ∆ерар вводит объективный критерий дл€ установлени€ химических формул Ч они должны соответствовать четырем объемам. Ќо это положение он дополн€ет правилом: в формуле органического соединени€ число атомов углерода должно делитьс€ на 4(— = 6), или на 2 (— = 12), число атомов водорода Ч на 4, а число атомов кислорода Ч на 2. Ёто так называемый закон четности или закон четных паев. ¬ действительности это правило справедливо только дл€ соединений, не содержащих азота. ќно €вл€етс€ следствием удвоени€ формул органических соединений, не содержащих азота. ќно €вл€етс€ следствием удвоени€ формул органических соединений, четырехвалентности атома углерода и четности суммы всех единиц валентностей атомов элементов, образующих соединений.
Ќова€ классификаци€ органических соединений, по мнению ∆ерара, должна исходить, во-первых, из правильных химических формул (четырехобъемных) и, во-вторых, устанавливать формулы надо путем постепенного разрушени€ более сложных объединений. Ёти принципы классификации ∆ерар развил и применил в Ђ ратком учебнике органической химииї [12].
√лавным же выводом рассматриваемой работы ∆ерара €вилось предложение унифицировать все формулы органических соединений, а именно: считать объемы молекул всех соединений в газообразном состо€нии одинаковыми. ќдновременно он предлагал изменить атомные веса (Ђэквивалентыї) некоторых элементов, например, следующим образом:

ќн предлагал изменить атомные веса (Ђэквивалентыї) некоторых элементов
—огласно новым эквивалентам воды и кислорода (по сравнению с эквивалентом водорода 12,5), пишет он, Ђплотности простых газов станов€тс€ пропорциональными их эквивалентамї [9, т. I, 314].
Ќесмотр€ на то, что ∆ерар смешивал пон€ти€ Ђэквивалентї, Ђатомный весї и Ђмолекул€рный весї, этот весьма важный вывод способствовал сближению его новых Ђэквивалентовї с атомными весами Ѕерцелиуса (1826) и возрождению объемного метода јвогадро. ∆ерар пришел к этому стихийно, исход€ из чисто химических соображений в области органической химии. ≈го система атомных весов и химических формул €вилась следствием развити€ унитарных идей Ћорана и ƒюма.
ак мы уже писали, новые идеи ∆ерара были прин€ты в штыки ѕарижской академией наук (стр. 23). Ѕерцелиус в годовом отчете об успехах химии посв€тил работе ∆ерара несколько полных пренебрежени€ строчек: Ђ∆ерар примен€ет весьма удобный метод создавать теории, главное преимущество которого состоит в том, что все известные факты, которые не согласуютс€ с его теорией, объ€вл€ютс€ невернымиї [1, стр. 327]. —толь отрицательное отношение Ѕерцелиуса объ€сн€етс€ тем, что идеи ∆ерара расшатывали все здание дуализма, хот€ предложенные им атомные веса были близки к атомным весам Ѕерцелиуса.
Ѕолее странным кажетс€ отношение ƒюма, который предложил ∆ерару выбросить всю теоретическую часть его статьи. ¬едь ƒюма был одним из первых, кто выступил против электрохимической теории Ѕерцелиуса, он был единственным членом академии, понимавшим передовое значение идей ∆ерара дл€ развити€ унитарного направлени€.
∆ерара поддержали только его друзь€ Ч ћалагути и аур (с Ћораном ∆ерар тогда еще не был знаком). ѕравда, аур указал ∆ерару на то, что форма изложени€ его статьи производит отрицательное впечатление. аур, очевидно, имел в виду нескромность и категоричность выражений ∆ерара Ч Ђ€ утверждаюї, Ђ€ доказываюї, Ђэтот атомный вес неверенї, Ђданна€ формула ложнаї и т. д. ћногие общеприн€тые формулы ∆ерар объ€вл€л неверными, не учитыва€ того, что некоторые из них были установлены членами академии, слушавшими его выступление. “ак, например, он объ€вил ошибочными формулы стрихнина и кодеина, установленные –еньо, чем тот, конечно, был возмущен. Ќо все же истинными причинами враждебного отношени€ к прогрессивным иде€м ∆ерара были косность и рутина большинства академиков, которые не представл€ли себе химию без дуализма.
»х враждебное отношение не остановило ∆ерара, он продолжал развивать свои идеи, будучи твердо убежденным в их правильности. ¬ €нваре 1843 г. он сообщает ауру о том, что несколько изменил свою систему эквивалентов: Ђћои идеи об эквивалентах были бы, возможно, лучше прин€ты, если вместо того, чтобы исходить из органической химии, € исходил бы из минеральной химии, ибо € должен был сохранить ќ = 100. Ќо тогда пришлось бы уменьшить вдвое почти все наши формулы органической химии. ¬от, например, несколько тел, выраженных таким образом согласно истинным эквивалентам (...)
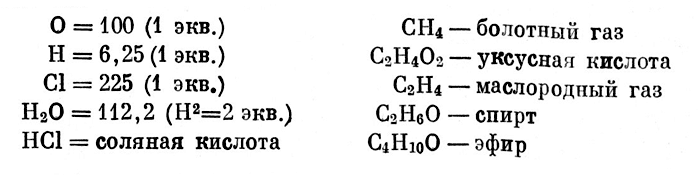
¬от, например, несколько тел, выраженных таким образом согласно истинным эквивалентам
¬ы позже увидите, что € правї [9, т. II, стр. 29]. «десь ∆ерар впервые предлагает исходить из двухобъемных формул дл€ всех соединений и в св€зи с этим уменьшить вдвое общеприн€тые тогда формулы большинства органических соединений.
¬ этом же письме ∆ерар касаетс€ статьи ƒюма [14] о гомологии жирных кислот, опубликованной в но€бре 1842 г., т. е. после статьи ∆ерара: Ђ«акон ƒюма о жирных кислотах полностью согласуетс€ с моими иде€ми. ѕо его мнению, эти кислоты образуютс€ добавлением или отн€тием —4Ќ4 (¬ современных обозначени€х C1H4 соответствует —Ќ2) (—4 = 1 экв., Ќ4 = 2 экв.), а ¬ы ведь знаете, что в телах, не содержащих азота, € всегда допускаю четное число эквивалентов водорода, так как этот водород происходит из воды (Ќ4O2)ї [9, т. II, стр. 29]. ¬ мае 1843 г. ƒюма опубликовал более подробное исследование об органических кислотах [15], где указал, что его выводы согласуютс€ с выводами ∆ерара. ѕо мнению “иффено, ƒюма пришел к открытию гомологии жирных кислот под вли€нием системы эквивалентов ∆ерара и предполагает, что ƒюма узнал об этой системе еще в июле 1842 г. от аура которому ∆ерар писал о ней в мае того же года [9, т. 2, стр. 18].
¬торую статью на эту же тему ∆ерар опубликовал в июне 1843 г. ¬ ней он подробно изложил свою систему в новом виде. ќн сообщает, что из его исследований вытекают два вывода: Ђили H4O2 и C4O2 выражают один эквивалент, или они выражают два эквивалента. ¬ случае первой гипотезы надо было бы удвоить формулы минеральной химии дл€ того, чтобы они согласовывались с органическими формулами; во втором случае надо было бы уменьшить вдвое большинство формул органических соединенийї [9, т. 1, стр. 316]. —ам ∆ерар склон€етс€ ко второму выводу, ибо формулы органических соединений удваивались искусственно из-за дуалистического подхода к строению (конституции, как тогда говорили) солей. “ак критическое отношение к принципам дуализма привело ∆ерара к правильному решению.
ƒл€ установлени€ формулы уксусной кислоты, пишет он, исходили из количества серебра, получаемого при прокаливании уксуснокислого серебра. ќтсюда определ€ли вес Ђэквивалентаї окиси серебра, приписыва€ ей формулу AgO: Ђэквивалентї соли устанавливали, счита€ соль состо€щей из окисла и Ђкислотыї. “ак, формулу уксуснокислого серебра изображали —4Ќ6O3ХAgO(C4H6O4Ag), приписыва€ серебру удвоенный атомный вес. Ђ≈сли бы считали формулу воды и формулу соответствующих окислов металлов R2O, а не RO, то наиболее естественный путь, по которому надо следовать, например в случае уксусной кислоты, Ч это считать эквивалентом органического вещества то количество соли, которое содержит один эквивалент металла (половину R2): уксусна€ кислота —2Ќ4O2; уксуснокислое серебро C2(H3Ag)O2; хлоруксусна€ кислота —2(—l3Ќ)O2; хлоруксусное серебро C2(Cl3Ag)O2ї [9, т. I, стр. 317]. ∆ерар указывает, что новые формулы говор€т в пользу водородной теории кислот, ибо, например, нова€ формула хлоруксусной кислоты €сно показывает, что нельз€ допускать предсуществование воды в кислоте, а нова€ формула уксуснокислого серебра Ч на невозможность существовани€ в нем окиси серебра, ибо окись серебра имеет формулу Ag2O.
∆ерар, конечно, ошибалс€, приписыва€ всем окислам металлов формулу R2O, по аналогии с Ќ2O, но то, что он в принципе признал возможность существовани€ таких окислов, привело ко многим важным следстви€м. ѕрежде всего это помогло ему правильно разграничить кислоты по их основности. ѕоскольку хлористоводородна€, бромистоводородна€, азотна€ кислоты Ч одноосновны, он предложил уменьшить прин€тые дл€ них формулы вдвое (Ќ—l, Ќ¬r, HNO3, вместо Ќ2—l2, H2Br2, N2H2O6). ƒалее ∆ерар приводит следующую таблицу:

ƒалее ∆ерар приводит следующую таблицу
ЂЌадо полностью изменить наши определени€ кислот и солей, Ч пишет он. Ч я называю солью вс€кую молекул€рную систему, заключающую определенное число эквивалентов водорода или металла, которые могут быть замещены непосредственно или путем двойного разложени€ таким же числом эквивалентов другого металла или водорода. Ёквиваленты водорода или металла, которые могут таким образом замещатьс€, называютс€ основанием солиї lї, [9, т. 1, стр. 321]. ќдноосновные соли содержат один эквивалент металла, двуосновные - два и т. д. “аким образом, терар причисл€ет кислоты к сол€м, ибо, последовательно фимен€€ теорию типов ƒюма, считает, что кислоты и соли принадлежат к одному и тому же типу. ќснованием н считает не окислы металлов, а металлы или водород. »деи водородной теории кислот ∆ерар развивает более последовательно, чем Ћибих. ≈сли последний ограничилс€ только органическими кислотами, то ∆ерар, не признава€ теории радикалов и рассматрива€ кислоты и соли унитарно, не видит причин не примен€ть водородную теорию ко всем кислотам. ∆ерар идет дальше и в вопросе об основности кислот. Ћибих считал серную хромовую и угольную кислоты одноосновными и рассматривал их кислые соли как соединени€ одной молекулы соли одной молекулой кислоты, ∆ерар же, исход€ из своей системы, делает правильный вывод о двуосновности указанных кислот и правильно объ€сн€ет состав их кислых солей.
—реди интересных выводов второй статьи находим, между прочим, такие: Ђјтомы, эквиваленты и объемы Ч синонимыї. Ђѕлотности газов пропорциональны их эквивалентамї. ≈ще в первой статье ∆ерар писал, что благодар€ его системе химических формул Ђисчезает противоречие между теорией эквивалентов и теорией объемов. ѕо-моему, вода состоит из 2 эквивалентов или объемов водорода и 1 эквивалента или объема кислородаї [9, т. II, стр. 20]. ќн делает вывод, что эквиваленты и простых и сложных тел соответствуют одинаковому объему (сложные вещества Ч 2 объемам, а простые Ч одному). ќн называет эти числа эквивалентами, ибо они получены на основе эмпирических данных о химических реакци€х веществ, а не на основе каких-либо гипотез. » поскольку система атомных весов Ѕерцелиуса исходила из объемных данных, то, естественно, ∆ерар не видит теперь никакого различи€ между атомами и эквивалентами.
—ледует заметить, что в то врем€ существовали три разных подхода к вопросу о химических обозначени€х. Ѕыли сторонники системы атомных обозначений, признававшие объемные данные или не признававшие их, сторонники системы эквивалентов, категорически не признававшие объемных данных, и, наконец, сторонники системы объемных обозначений, признававшие только объемные данные без какой-либо атомистической интерпретации (например, √ей-Ћюссак). ∆ерар видел достоинство своей системы в том, что она примирила все три точки зрени€, стерла грань между пон€ти€ми Ђэквивалентї, Ђатомї и Ђобъемї. «десь надо, конечно, отметить, что первое пон€тие отличалось от современного. ѕод эквивалентами понимали Ђсоединительные весаї, определ€емые химическим путем, и, естественно, эквиваленты многих веществ совпадали с их атомными весами. “ак получилось и тогда, когда ∆ерар изменил некоторые значени€ этих эквивалентов дл€ неметаллов (ќ, —, S): их атомные веса и эквиваленты стали тождественными. Ќо если с неметаллами все оказалось благополучным, то изменени€, предложенные ∆ераром дл€ металлов, были неудачными. јтомные веса многих металлов оказались равными их эквивалентам, так как ∆ерар изображал формулы низших окислов всех металлов как R2O. ќтсюда €сно, что изменени€, предложенные ∆ераром, были удачными только дл€ щелочных металлов. “аким образом, атомные веса ∆ерара приблизили его систему к системе Ѕерцелиуса (за исключением атомных весов металлов).
¬ывод ∆ерара о том, что плотность газов пропорциональна их Ђэквивалентамї (молекул€рному весу), €вл€етс€ важным шагом вперед, при этом данное положение он распростран€ет на все газообразные соединени€. онечно, его подход к этому вопросу недостаточно последователен, ибо, как мы уже говорили, определ€€ атомный вес элементов, он исходил из одного объема, а устанавлива€ формулы сложных веществ, считал молекул€рный объем соединений равным двум.
»звестный интерес представл€ет метод определени€ молекул€рной формулы и молекул€рного веса органических веществ, описанный ∆ераром в его Ђ ратком учебникеї. ƒл€ этого определени€ ∆ерар рекомендовал пользоватьс€ не только химическими методами (изучение реакций замещени€, соединени€ и разложени€), но и физическим, основанным на измерении плотности веществ в газообразном состо€нии. ќн писал: Ђ”же давно с успехом пользуютс€ определением плотности паров летучих неразлагающихс€ веществ. ƒл€ того чтобы полученное опытное число согласовалось с формулой вещества, необходимо, чтобы сумма плотностей элементов данного вещества была бы почти в два раза больше этого числа. “огда говор€т, что эквивалент вещества представл€ет два объема паров. ≈сли, например, формула вещества —2Ќ6ќ, тогда мы имеем:

≈сли, например, формула вещества —2Ќ6ќ, тогда мы имеем
—умма 3,165⁄2=1,582 должна совпадать с числом, полученным непосредственно дл€ плотности вещества, если прин€та€ формула правильнаї [12, стр. 57].
“аким образом, определ€€ молекул€рный вес сложного вещества, ∆ерар исходил не из его плотности в газообразном состо€нии (как делаетс€ теперь), а из относительной плотности элементов по воздуху. ѕодобно ƒюма, он складывает значени€ плотности элементов согласно своей эмпирической формуле. Ќо предшественники ∆ера-ра дл€ согласовани€ теоретических данных с опытными делили сумму значений плотности обычно на 2 или на 4, ∆ерар же предлагает делить эту сумму всегда на два, и если результат не совпадает с опытными данными, то надо изменить формулу вещества. “акой метод определени€ молекул€рного веса до некоторой степени произволен, так как зависит от точности анализа и от гипотетической плотности пара некоторых элементов (—, S, P, As, Si и т. д.).
»так, предлага€ свою систему атомных весов и химических формул, ∆ерар стихийно признал основные положени€ гипотезы јвогадро о равенстве числа молекул в единице объема, а также его метод определени€ молекул€рного веса газообразных веществ. ќднако ∆ерар еще не различал пон€тий Ђатомї и Ђмолекулаї простых веществ; работы јвогадро, јмпера и √одена ему, очевидно, не были знакомы.
”потребл€€ нечеткую терминологию, смешива€ атом с эквивалентом и называ€ эквивалентом и атомный и молекул€рный вес. ∆ерар затемн€л смысл своих идей, что очень преп€тствовало их воспри€тию. ѕравильному разграничению основных пон€тий атомно-молекул€рного учени€ и распространению гипотезы јвогадро на простые вещества много содействовал Ћоран. ќн неоднократно указывал ∆ерару на слабые места его системы, подсказывал ему направление, в котором ее надо развивать. √лавным недостатком системы ∆ерара Ћоран считал ее непоследовательность в применении принципа единой объемной основы. Ђћне кажетс€, Ч пишет он ∆ерару, Ч что надо все свести к единице объема и выражать тела так:
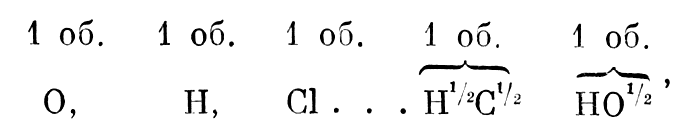
ћне кажетс€, Ч пишет он ∆ерару, Ч что надо все свести к единице объема и выражать тела так
т. е. показать, что соединение образовано путем реакции двойного разложени€ (или сгущени€) простых реагирующих веществ... јтомы должны быть делимы. ¬ы мне возразите, что ¬ы против дробей. Ќо их можно избежать, употребл€€ какое-то условное обозначениеї [9, т. I, стр. 22]. “аким образом, примен€€ ту же нечеткую терминологию, которой в свое врем€ пользовалс€ ƒюма, говор€ об атомах и полуатомах, Ћоран фактически подходит к мысли о том, что простые газы состо€т из двухатомных молекул.
¬ более позднем письме Ћоран развивает эту идею, употребл€€ теперь термин молекула и полумолекула: Ђ»з правила о посто€нной четности числа эквивалентов € прихожу к важному следствию о расположении атомов. (¬ы только не пугайтесь этого слова.) ¬одород, хлор, азот, металлы имеют двойные молекулы. ≈сли отнимают половину одной из этих молекул, надо ее об€зательно заменить полумолекулой другого тела этой же группыї [9, т. I, стр. 81]. Ђ—уществует различие между 1 объемом кислорода и 1 объемом хлора, водорода, азота... в реакцию никогда не вступает один объем хлора, водорода, но всегда два объема, из которых, правда, один может быть замещен веществом того же семейства: H2, (Ќ—l), (ће—l) и т. д. Ёто точно, что нельз€ замещать Ќ через ќ. ќдним словом, Ќ не €вл€етс€ эквивалентом ќ. Ёто смешение происходит, возможно, из-за нечеткости формулировокї [9, т. I, стр. 103].
«десь Ћоран впервые разграничивает пон€ти€ Ђэквивалентї и Ђатомї. Ѕолее подробно этот вопрос Ћоран рассматривает в письме от 6.IV 1846 г.: Ђя вам, кажетс€, говорил, что не понимаю, почему только металлы привиле-гированы в том смысле, что могут иметь два эквивалента? я думаю, что это же должно быть и у неметаллических тел. я много думал об эквивалентах. —лова Ђэквивалентыї, Ђатомыї, Ђобъемыї не могут быть синонимами. —уществуют тела, между которыми нет эквивалентности... —уществует эквивалентность между ќ, S, Se, “е; существует эквивалентность между Ќ, —l, ¬r, металлами. Ќо эти группы между собой не эквивалентны: здесь есть атомы, пропорциональные числа, но нет эквивалентовї [9, т. I, стр. 201]. Ћоран фактически подошел к пониманию различной валентности элементов, хот€ и не выразил этого четко. –азграничение пон€тий Ђатомї и Ђэквивалентї привело Ћорана к пересмотру вопроса об объемах, соответствующих простым веществам. ќн предлагает относить пон€тие Ђобъемї только к пон€тию Ђатомї. ЂЁквивалент <...> это количество простого вещества, которое при замещении другого простого вещества играет его роль. Ќе все простые вещества эквивалентны <...> Ёквивалент и атом не €вл€ютс€, таким образом, синонимамиї [9, т. I, стр. 204Ч205]. ¬ таблице атомов Ћоран подраздел€ет их на две подгруппы: Ђмонадыї и Ђдиадыї; первые, по его мнению, могут существовать в виде одного атома, а вторые (диады) только в виде двух атомов. Ёти группы соответствуют нашим современным представлени€м об элементах с четной и нечетной валентностью. ¬от таблица Ћорана
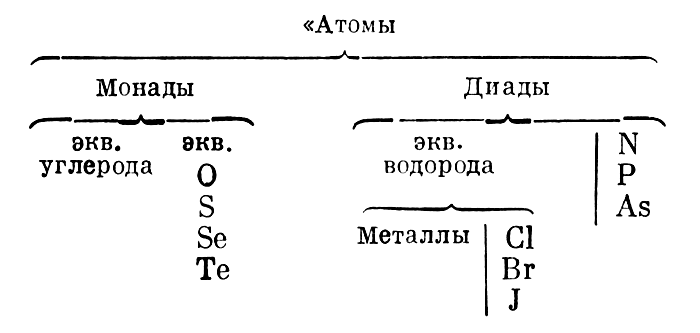
¬от таблица Ћорана
ƒопустим, что один объем содержит один атом и что каждый атом €вл€етс€ бинарным
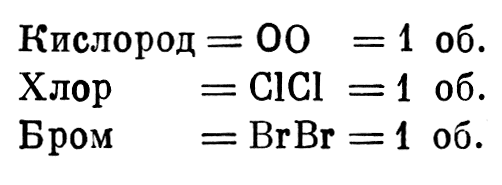
ƒопустим, что один объем содержит один атом и что каждый атом €вл€етс€ бинарным
¬от что происходит между хлором и водородом:
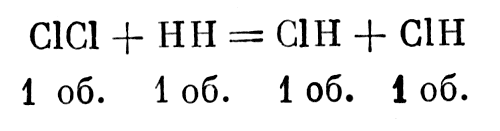
¬от что происходит между хлором и водородом
ƒиады всегда существуют только в четном числе (атомов)... ¬ то же врем€ у монад молекула така€ же, как у диад, но она может существовать половинкой (в виде одного атома. Ч ћ. ‘.) без замещени€ї [9, т. I, стр. 205].
¬ этой таблице Ћоран считает водород Ђамфиднымї: атом водорода может замещатьс€ и атомом металла, и атомом галогена.
»де€ Ћорана о диадах и монадах исходит из правила четности ∆ерара, которое Ћоран дополнил правилом азота [34]. —огласно объединенному правилу, число атомов углерода и кислорода в органическом соединении (в современных формулах) может быть либо четным, либо нечетным, в то врем€ как число атомов водорода всегда должно быть четным. ≈сли же соединение содержит и азот, то сумма атомов водорода и азота (или фосфора, мышь€ка) должна делитьс€ на два. ¬последствии идеи Ћорана в более четкой форме высказал анншщаро [35], который доказал, что элементы и радикалы с четной валентностью могут существовать в свободном виде, а элементы или радикалы с нечетной валентностью в свободном виде существовать не могут. ¬ 1869 г. Ѕломстранд создал свою классификацию элементов, подраздел€€ их на элементы с четной и нечетной валентностью [36].
—вои идеи Ћоран подробно изложил в статье, опубликованной осенью 1846 г. ќн пишет: Ђ≈сли вместо того, чтобы вз€ть, как ∆ерар, один объем дл€ простых тел и два объема дл€ сложных, мы выразим все тела как простые, так и сложные, одним объемом, мы получим более правильное обозначение <...> ћы допускаем, что кажда€ молекула простого тела делитс€ по меньшей мере на две части, которые мы можем назвать атомами <...> јтом ∆ерара представл€ет наименьшее количество простого тела, которое может существовать в соединении. ћо€ молекула (простого вещества) представл€ет наименьшее количество простого тела, которое необходимо вз€ть дл€ получени€ соединени€ и которое делитс€ на две части во врем€ самой реакции. “ак, хлор может входить в соединение, но дл€ образовани€ этого соединени€ надо вз€ть —l2ї [34, стр. 295Ч296]. ак довод в пользу своих идей Ћоран приводит пон€тие об активности веществ в момент выделени€: Ђ≈сли привести в соприкосновение две свободные молекулы брома и водорода (BrBr1) и (HH1), то сродство ¬r к Br1 и Ќ к H1, возможно, €вл€етс€ достаточным, чтоб воспротивитьс€ соединению ¬r и Br1 с Ќ и H1. Ќо если мы имеем в наличии только ¬r + Ќ, то ввиду того, что эти два тела (атома. Ч ћ. ‘.) не должны разрушать никакого сродства, они могут очень легко соединитьс€ї [34, стр. 297].
Ёти цитаты вы€вл€ют то новое, что внес Ћоран в систему ∆ерара. „исто химическим путем он пришел к необходимости четкого разграничени€ пон€тий Ђатомї, Ђмолекулаї, Ђэквивалентї, к более последовательному применению гипотезы јвогадро. » его путь к идее о ƒвуатомности молекул элементарных газов был вполне самосто€тельным. “олько впоследствии он подкрепил свои выводы ссылкой на гипотезу јмпера, который высказал в 1814 г. те же мысли, что и јвогадро, но трем€ годами раньше.
»деи Ћорана нашли свое отражение в новом учебнике ∆ерара [16], где ∆ерар поместил специальное посв€щение Ћорану:
Ђƒругу моему ќгюсту Ћорану, члену-корреспонденту јкадемии.
ѕосв€ща€ ¬ам эту книгу, € хочу напомнить читателю, сколько хорошего в ней принадлежит ¬ам, и живейшее уважение, которое € чувствую к ¬ам.
Ў. ∆ерарї
¬ этом учебнике ∆ерар уже не считает молекулу и эквивалент синонимами. Ђћы рассматриваем вс€кое тело, Ч пишет он, Ч как строение, как унитарную систему, образованную соединением в определенном, но неизвестном пор€дке, бесконечно малых и неделимых частиц, называемых атомами. Ёта система называетс€ частицей (molecule) тела. ¬ частице простого тела и атомы однородны или однокачественны, т. е. современна€ наука не видит пока никакой разницы. ¬ частице сложного тела атомы разнородны и разнокачественны <...> ¬ажно установить различие между словами: атом и молекула, потому что часто их смешивают в сочинени€х по химии. јтом неделим, но он и не существует в отдельном состо€нии; молекула есть группа атомов, держащихс€ вместе прит€жением материи. Ёта группа делима нашими химическими или механическими средствами, но только до известной степени: частица должна состо€ть по меньшей мере из двух атомовї [16, стр. 32, 33]. ћы видим, что ∆ерар уже четко разграничивает пон€ти€ Ђатомї, Ђмолекулаї и Ђэквивалентї, указывает, что величина эквивалента сложного вещества зависит от того, Ђкакому другому телу, каким отправлени€м (реакци€м. Ч ћ. ‘.), каким свойствам соответствует этот эквивалентї, признает, что один и тот же элемент может иметь два эквивалента или несколько. ѕри вод€ формулы кислот —lЌ, SO4H2, –O4Ќ3, он подчеркивает, что эквивалентные количества этих кислот будут —lЌ, 1/2[SO4Ќ2], 1/3[PO4H3]. Ђ’имические обозначени€ не всегда могут изображать эквиваленты, потому что эти I последние измен€ютс€, смотр€ по химическим функци€мї [16, стр. 68].
’от€ ∆ерар под вли€нием Ћорана и признал, что молекулы простых веществ состо€т из атомов одного рода, но он не высказалс€ достаточно четко о числе атомов, вход€щих в состав таких молекул. Ќапример, обсужда€ образование —ќ из элементов, он пишет: Ђ≈сли представить это графически, молекула углерода была бы результатом прит€жени€ четырех сфетических атомов, сгруппированных так:

≈сли представить это графически, молекула углерода была бы результатом прит€жени€ четырех сфетических атомов, сгруппированных так
ћолекула кислорода состо€ла бы из следующих групп:
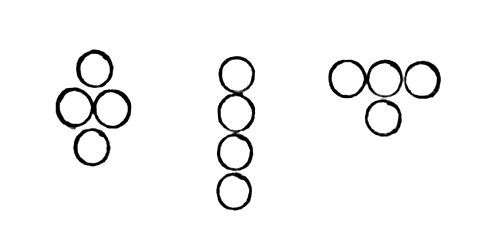
ћолекула кислорода состо€ла бы из следующих групп
тогда молекула, составленна€ из атомов разного рода (из атомов кислорода и углерода), могла бы иметь одну из следующих форм:
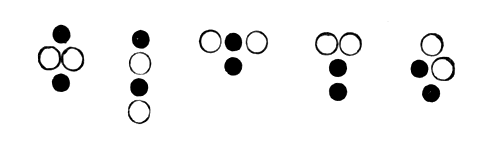
“огда молекула, составленна€ из атомов разного рода (из атомов кислорода и углерода), могла бы иметь одну из следующих форм
ѕри химическом соединении молекулы обмениваютс€ своими атомами. огда углерод и кислород соедин€ютс€, то частицы угл€ обменивают известное число атомов углерода на известное число атомов кислорода и обратної [16, стр. 33].
онечно, такое графическое изображение - не более как дидактическа€ модель, но она хорошо по€сн€ет идею жерара о том, что все реакции надо считать реакци€ми двойного обменного разложени€, и эта иде€ вытекает из нового пон€ти€ о молекуле простых веществ. роме того, эти модели подчеркивают отсутствие принципиального различи€ между молекулами простых и сложных веществ. ак видно из этих моделей, ∆ерар допускает многоатомность молекулы кислорода, не счита€ при этом окончательно установленным, что она состоит именно из двух атомов. (Ќадо отметить, чтотакой категоричности не было и у јвогадро, хот€ он считал молекулу кислорода двухатомной).
¬ новом учебнике ∆ерар называет атомный и молекул€рный вес Ђпропорциональными числамиї, а не эквивалентами, как называл в ЂPrecisї; метод определени€ молекул€рного веса одинакив в обоих учебниках.
ќсновные положени€ своей системы ∆ерар излагает в IV томе Ђ урса органической химииї [20]. ¬ первых трех томах он еще пользуетс€ системой эквивалентов, но все химические формулы сводит к одинаковому объему (4 объема). “олько в IV томе он примен€ет свои атомные веса и двухобъемные формулы. ќчевидно, ∆ерар поступил так, жела€ облегчить р€довым химикам усвоение новых формул, Ч ведь больше всего нареканий вызывала его попытка заменить ими общеприн€тые эквиваленты ( ак мы говсрили, ∆ерар хотел применить новую систему атомных весов в немецком переводе своего учебника [21]. ќднако перевод вышел в том же виде, что и оригинал.).
Ћоран тоже советовал ∆ерару не настаивать из-за тактических соображений на новой системе атомных весов; главное внимание следует обратить на исправление неверных химических формул, тех, которые не удовлетвор€ют правилу четности. Ђћожете ли ¬ы удовлетворитьс€ тем, Ч спрашивает Ћоран друга, Ч что ¬ы будете говорить, вид€ какую-нибудь формулу: Ђќна невернаї, не указыва€ на то, что ¬аши эквиваленты привели ¬ас к этому выводу?ї [9, т. 1, стр. 26]. —ам Ћоран не решалс€ сразу перейти к Ђэквивалентамї ∆ерара и до 1845 г. пользовалс€ эквивалентами ƒюма.
—ледует отметить, что во ‘ранции нова€ система обозначений ∆ерара не преподавалась вплоть до 1863 г., когда ƒелаво (Delavaud), профессор “улонской морской медицинской школы, первым заговорил о ней с кафедры. ƒва года спуст€ по€вилась книга Ќаке (јльфред ∆озеф ѕапе (1834-1916) - врач, химик, политический ве€тель, профессор медицинского факультета в ѕариже; в 1869 г. лишен кафедры за свои левые, убеждени€. ¬ 1887 г. примкнул к реакционному движению генерала Ѕуланже, после его падении (в 1891 г.) отошел от политики) Ђѕринципы химии на основе современных теорийї [37] Ч первый учебник, составленный по системе ∆ерара.
¬ 1866 г. расстатьс€ с эквивалентами и применить новые атомные весы решилс€ наконец ¬юрц. ѕо этому поводу √римо пишет: Ђ≈сли бы он это сделал раньше, министр призвал бы его к пор€дкуї [1, стр. 433]. ќднако большинство химиков ‘ранции продолжали пользоватьс€ системой эквивалентов вплоть до конца XIX в. Ёмпирическое направление в химии, которое возглавл€л такой крупный ученый, как Ѕертло, бывший €рым противником атомно-молекул€рного учени€, сыграло в этом отношении отрицательную роль. ¬ других же странах переход к новой системе атомных весов и химических формул началс€ намного раньше. ¬ –оссии уже в 1850-х годах систему ∆ерара стали примен€ть Ѕекетов (1853) [38] ћенделеев (1856) [39], —околов (1859) [17] и др.
ѕосле международного конгресса химиков в арлсруэ (1860) система ∆ерара с предложенными иццаро исправлени€ми атомных весов металлов получила распространение в »талии, јнглии, а несколько позже ив √ермании. ¬ 1861 г. вышел учебник ћенделеева Ђќрганическа€ хими€ї, построенный по системе ∆ерара. ак отмечал в свое врем€ русский ученый, уиверждение этой ситемы на конгрессе в арлсруэ подготовило почву дл€ открыти€ периодического закона химических элементов.
|
ѕќ»— :
|
© NPLIT.RU, 2001-2021
ѕри использовании материалов сайта активна€ ссылка об€зательна:
http://nplit.ru/ 'Ѕиблиотека юного исследовател€'
ѕри использовании материалов сайта активна€ ссылка об€зательна:
http://nplit.ru/ 'Ѕиблиотека юного исследовател€'