
ПОСЛЕ БОРА
Несмотря на необычность постулатов Бора, его теория нашла довольно быстрое признание и достаточно много талантливых и сильных последователей. Если бы потребовалось определить отношение к ней физиков в те годы, то, пожалуй, пришлось бы назвать чувство облегчения, чувство освобождения от того постоянного напряжения, в котором все они до сих пор находились, пытаясь удержать в памяти разрозненные факты и хоть как-то связать концы с концами. Теперь все атомные явления, естественно, группировались вокруг непонятной, но простой модели; часть из них блестяще ею объяснялась, а другая требовала дальнейшего развития модели.
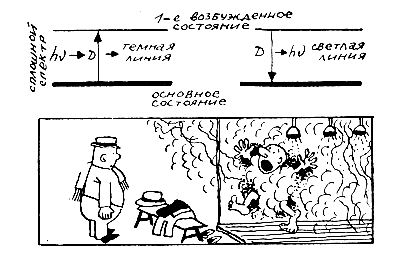
В частности, теперь очень просто можно было объяснить опыт Кирхгофа и Бунзена с парами натрия.
Действительно, пока луч от раскаленного тела не прошел через пары натрия, атомы которого находятся в основном состоянии, он содержит все длины волн. Проходя через пары, луч переводит атом натрия из основного состояния в первое возбуждение. На это затрачивается энергия кванта E = hν, частота которого ν как раз и совпадает с частотой линии D натрия. Поэтому прошедший свет уже не содержит лучей с этой частотой, и на шкале спектрографа мы видим сплошной спектр, перерезанный в желтой части темной линией D.
В обратном процессе, когда атомы натрия переходят из возбужденного состояния в основное, они излучают свет с той же частотой ν, которую прежде поглотили, то есть ту же линию D, но теперь уже ярко-желтую.
Несмотря на все успехи теории Бора, физики вначале принимали ее скорее как удобную модель, но не очень верили в реальность такой энергетической лестницы в атоме. Это сомнение разрешили Джеймс Франк (1882—1964) и Густав Герц (род. 1887) (племянник знаменитого Генриха Герца) в том же 1913 году. Как и всякая ясная идея, теория Бора не только объясняла старые факты, но также подсказывала пути для своей проверки.
Арнольд фон Зоммерфельд (1868—1951) — замечательный физик и блестящий педагог — был одним из первых в Европе, кто сразу же не только поверил в постулаты Бора, но и развил их дальше, «...следуя, как когда-то Кеплер при изучении планетной системы, внутреннему чувству гармонии». Он рассуждал так: если атом подобен солнечной системе, то электрон в такой системе может вращаться не только по окружности, как в модели Бора, но и по эллипсам, причем ядро должно находиться в одном из фокусов этих эллипсов.
Зоммерфельд
Эллипсы с одинаковой большой полуосью принадлежат одному и тому же значению главного квантового числа n, так как энергии электрона на таких орбитах равны между собой (Зоммерфельд знал доказательство, а нам придется поверить в это). Однако эллипсы различаются по степени сплющенности, которая зависит от орбитального момента. Вполне в духе идей Бора Зоммерфельд предположил, что при заданном n эллипсы могут быть сплющены не произвольным образом, а только так, чтобы орбитальное квантовое число l (которое их различает) принимало целые значения l = 0,1,2,... n - 1, то есть число допустимых эллипсов не превышает числа n — номер стационарного состояния.
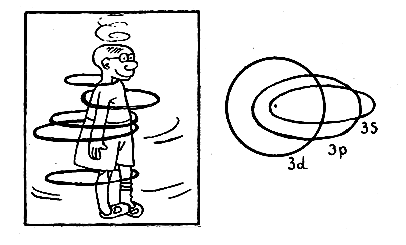
Орбитали
Бор и Зоммерфельд показали даже нечто большее: если учесть теорию относительности Эйнштейна, то окажется, что энергия электрона различна на всех эллипсах, а потому уровни энергии в атоме необходимо нумеровать двумя квантовыми числами: n и l. По той же причине спектральные линии, возникающие при переходах электрона между уровнями, с разными n, должны иметь тонкую структуру, то есть расщепляться на несколько компонент. По просьбе Зоммерфельда Фридрих Пашен проверил и подтвердил это следствие теории на примере линии гелия λ = 4686 Ǻ, которая соответствует переходу с уровня n = 4 на уровень n = 3 (с четвертого уровня на третий). Внимательно рассмотрев фотографию спектра гелия, он обнаружил, что линия в действительности состоит из тринадцати тесно расположенных линий.
Гелий
Это было удивительное совпадение, и в то время (1916 году) его сравнивали с вычислениями Леверье и Адамса, которые предсказали планету Нептун.
Но даже два квантовых числа — n и l не объяснили всех особенностей спектров. Например, если поместить излучающий атом в магнитное поле, то спектральные линии расщепляются совсем по-другому.
Расщепление спектральных линий в магнитном поле пытался обнаружить Фарадей еще в 1862 году в своей последней (уже неопубликованной) работе. Однако магнит, который он для этой цели использовал, был слишком слаб, и лишь в 1896 году Питер Зееман наблюдал явление, которое в свое время тщетно искал Фарадей.
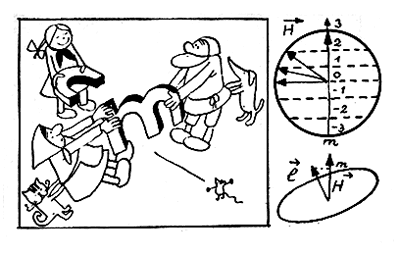
После работ Бора и Зоммерфельда явление расщепления спектральных линий в магнитном поле стали толковать следующим образом. Представьте, что перед вами электромотор. Даже не вникая в технические детали его устройства, вы со школьных лет знаете, что его ротор начнет вращаться, если через его обмотку пропустить электрический ток. Электрон, движущийся в атоме по замкнутой орбите, подобен витку тока в обмотке электромотора. И точно так же, как этот виток, орбита электрона в магнитном поле начнет поворачиваться. Однако в отличие от витка она не может занимать в атоме произвольные положения, поскольку этому препятствуют квантовые законы. Суть этих квантовых законов проще всего понять, взглянув на прилагаемый рисунок. На рисунке магнитное поле направлено снизу вверх, а орбита электрона изображена «с ребра», причем радиус орбиты численно равен значению орбитального момента l (на рисунке l = 3). Оказывается, законы квантования допускают только такие положения плоскости орбиты относительно магнитного поля Я, при которых проекция диаметра орбиты на направление поля H равна целому числу. Это третье магнитное квантовое число m, как легко видеть, принимает значения m = l, l — 1,..., 1, 0, — 1,..., — (l—1), — l, то есть всего (2l+ 1) значений.
Таким образом, в магнитном поле каждый уровень Enl с заданными значениями квантовых чисел n и l расщепится еще на (2l+ 1) подуровня, Enlm, каждый из которых однозначно определяется заданием трех целых квантовых чисел: n, l, m. А это, мы знаем, приводит к дополнительному расщеплению спектральных линий.
Усложняясь, теория Бора постепенно теряла свое первоначальное изящество и наглядность. На ее место пришла формальная модель атома, от которой требовалось лишь одно: дать правильную систематику термов. Термин «квантование» постепенно потерял свой прежний смысл: им обозначали теперь формальный процесс сопоставления целых (квантовых) чисел n, l и m каждому уровню энергии в атоме, а точнее, тому типу движения, в котором находится электрон. Квантовые числа n, l и m определяют стационарные орбиты в изолированном атоме. Внешние поля (электрическое и магнитное) влияют на движение электрона в атоме (расщепление уровней энергии), а это сразу же сказывается на структуре светового сигнала, который испускает атом (расщепление спектральных линий).
|
ПОИСК:
|
© NPLIT.RU, 2001-2021
При использовании материалов сайта активная ссылка обязательна:
http://nplit.ru/ 'Библиотека юного исследователя'
При использовании материалов сайта активная ссылка обязательна:
http://nplit.ru/ 'Библиотека юного исследователя'