
ŔŇÎĚŰ
 íŕ÷ŕëĺ âĺęŕ â ôčçčęĺ áűňîâŕëč ńŕěűĺ đŕçíűĺ č ÷ŕńňî ôŕíňŕńňč÷ĺńęčĺ ďđĺäńňŕâëĺíč˙ î ńňđîĺíčč ŕňîěŕ. Íŕďđčěĺđ, Ëčíäĺěŕí, đĺęňîđ Ěţíőĺíńęîăî óíčâĺđńčňĺňŕ, â 1905 ăîäó óňâĺđćäŕë, ÷ňî «...ŕňîě ęčńëîđîäŕ čěĺĺň ôîđěó ęîëüöŕ, ŕ ŕňîě ńĺđű — ôîđěó ëĺďĺřęč». Íî áîëüřčíńňâî ôčçčęîâ ďđčřëî ę âűâîäó, ÷ňî ďđŕâ Äć. Äć. Ňîěńîí: ŕňîě — ýňî đŕâíîěĺđíî çŕđ˙ćĺííűé ďîëîćčňĺëüíűé řŕđ äčŕěĺňđîě ďđčěĺđíî 10-8 ńě, âíóňđč ęîňîđîăî ďëŕâŕţň îňđčöŕňĺëüíűĺ ýëĺęňđîíű (čëč ęîđď¸ńëč, ęŕę ďčńŕëč â đóńńęčő čçäŕíč˙ő íŕ÷ŕëŕ âĺęŕ), đŕçěĺđű ęîňîđűő đŕâíű ďđčěĺđíî 10-13 ńě. Ńŕě Äćč-Äćč — ęŕę ĺăî íŕçűâŕëč ó÷ĺíčęč — îňíîńčëń˙ ę ńâîĺé ěîäĺëč áĺç ýíňóçčŕçěŕ.
Ŕ íĺęîňîđűĺ ôčçčęč ďđĺäńňŕâë˙ëč ńĺáĺ ŕňîě ńîâńĺě číŕ÷ĺ. Îäíč îá ýňîě ăîâîđčëč âńëóő. Ńđĺäč íčő áűëč Äćîíńňîí Ńňîíĺé, ďđĺäďîëŕăŕâřčé ĺůĺ â 1891 ăîäó, ÷ňî «...ýëĺęňđîíű äâčćóňń˙ âîęđóă ŕňîěŕ, ďîäîáíî ńďóňíčęŕě ďëŕíĺň», Ćŕí Ďĺđđĺí, ęîňîđűé â 1901 ăîäó ďűňŕëń˙ ďđĺäńňŕâčňü ńĺáĺ «íóęëĺŕđíî-ďëŕíĺňŕđíóţ ńňđóęňóđó ŕňîěŕ»; ˙ďîíńęčé ôčçčę Íŕăŕîęŕ č ńýđ Îëčâĺđ Ëîäć, óňâĺđćäŕâřčĺ â 1902 ăîäó, ÷ňî «...ďđîńňđŕíńňâŕ âíóňđč ŕňîěŕ ÷đĺçâű÷ŕéíî ăđîěŕäíű ďî ńđŕâíĺíčţ ń âĺëč÷číŕěč ńŕěčő îáđŕçóţůčő ĺăî ýëĺęňđč÷ĺńęčő ˙äđűřĺę — číűěč ńëîâŕěč, ŕňîě ďđĺäńňŕâë˙ĺň ńâîĺăî đîäŕ ńëîćíóţ ŕńňđîíîěč÷ĺńęóţ ńčńňĺěó, ďîäîáíóţ ęîëüöó Ńŕňóđíŕ».
Äđóăčĺ, íŕďđčěĺđ Ďĺňđ Íčęîëŕĺâč÷ Ëĺáĺäĺâ, äîâĺđ˙ëč ďîäîáíűĺ ěűńëč ňîëüęî ńâîĺěó äíĺâíčęó.  1887 ăîäó ĺěó ęŕçŕëîńü, ÷ňî ÷ŕńňîňŕ čçëó÷ĺíč˙ ŕňîěîâ îďđĺäĺë˙ĺňń˙ ÷ŕńňîňîé îáđŕůĺíč˙ ýëĺęňđîíŕ ďî îđáčňĺ. Ŕ ăîëîń Íčęîëŕ˙ Ěîđîçîâŕ áűë çŕďĺđň â ńňĺíŕő Ďĺňđîďŕâëîâńęîé ęđĺďîńňč.
Íî íč îäčí ńňîđîííčę čäĺč ďëŕíĺňŕđíîăî ŕňîěŕ íĺ ěîă îáú˙ńíčňü ăëŕâíîăî: óńňîé÷čâîńňč ńčńňĺěű, ńîńňî˙ůĺé čç ďîëîćčňĺëüíîé ńĺđäöĺâčíű č ýëĺęňđîíîâ, ęîňîđűĺ âîęđóă íĺĺ âđŕůŕţňń˙.
Äĺéńňâčňĺëüíî, íŕ ęđóăîâîé îđáčňĺ ýëĺęňđîí äâčćĺňń˙ óńęîđĺííî č, ńëĺäîâŕňĺëüíî, ďî ňĺîđčč Ěŕęńâĺëëŕ — Ëîđĺíöŕ, äîëćĺí ňĺđ˙ňü ýíĺđăčţ íŕ čçëó÷ĺíčĺ. Çíŕ˙ đŕçěĺđű ŕňîěŕ, ëĺăęî îöĺíčňü ńęîđîńňü äâčćĺíč˙ ýëĺęňđîíŕ ďî îđáčňĺ č âĺëč÷číó öĺíňđîńňđĺěčňĺëüíîăî óńęîđĺíč˙, îíî đŕâíî ďđčěĺđíî 1025 ńě/ńĺę2. Ďđč ňŕęîě óńęîđĺíčč čçëó÷ĺíčĺ äîëćíî áűňü íŕńňîëüęî číňĺíńčâíűě, ÷ňî óćĺ ÷ĺđĺç 10-8 ńĺę. ýëĺęňđîí îá˙çŕí óďŕńňü íŕ ďîëîćčňĺëüíűé öĺíňđ ďđčň˙ćĺíč˙, č ńčńňĺěŕ «ŕňîě» ďđĺęđŕňčň ńâîĺ ńóůĺńňâîâŕíčĺ.
Íč÷ĺăî ďîőîćĺăî â ďđčđîäĺ íĺ ďđîčńőîäčň: ŕňîě íĺ ňîëüęî óńňîé÷čâ, íî č âîńńňŕíŕâëčâŕĺň ńâîţ ńňđóęňóđó ďîńëĺ đŕçđóřĺíčé, ńâčäĺňĺëüńňâó˙ â ďîëüçó ěîäĺëč Ňîěńîíŕ. Îäíŕęî â ôčçčęĺ óćĺ áîëĺĺ äâóőńîň ëĺň ďđčí˙ňî ďđŕâčëî: îęîí÷ŕňĺëüíűé âűáîđ ěĺćäó ăčďîňĺçŕěč âďđŕâĺ ńäĺëŕňü ňîëüęî îďűň. Ňŕęîé îďűň ďîńňŕâčë â 1909 ăîäó Ýđíńň Đĺçĺđôîđä (1871 —1937) ńî ńâîčěč «ěŕëü÷čęŕěč».
Ďđĺäńňŕâüňĺ ńĺáĺ ęđóďíîăî č řóěíîăî ÷ĺëîâĺęŕ, ęîňîđűé ďđčíóćäĺí ńčäĺňü â ňĺěíîé ęîěíŕňĺ č, ăë˙ä˙ â ěčęđîńęîď, ń÷čňŕňü íŕ ýęđŕíĺ ńďčíňŕđčńęîďŕ âńďűřęč (ńöčíňčëë˙öčč) îň α-÷ŕńňčö. Đŕáîňŕ čçíóđčňĺëüíŕ˙: óćĺ ÷ĺđĺç äâĺ ěčíóňű ăëŕçŕ óńňŕţň. Ĺěó ďîěîăŕţň îďűňíűé čńńëĺäîâŕňĺëü Ăŕíń Ăĺéăĺđ (1882—1945) č äâŕäöŕňčëĺňíčé ëŕáîđŕíň Ýđíńň Ěŕđńäĺí (đîä. 1889). Čő ďđčáîđ íĺńëîćĺí: ŕěďóëŕ ń đŕäčĺě-Ń, čńďóńęŕţůčě α-÷ŕńňčöű, äčŕôđŕăěŕ, ęîňîđŕ˙ âűäĺë˙ĺň čç íčő óçęčé ďó÷îę č íŕďđŕâë˙ĺň ĺăî íŕ ýęđŕí čç ńĺđíčńňîăî öčíęŕ, č ěčęđîńęîď, ÷ĺđĺç ęîňîđűé íŕáëţäŕţň ńöčíňčëë˙öčč ŕ-÷ŕńňčö íŕ ýęđŕíĺ. Ěĺńňî ďî˙âëĺíč˙ î÷ĺđĺäíîé ńöčíňčëë˙öčč ďđĺäóăŕäŕňü íĺëüç˙ — îíč âîçíčęŕţň áĺńďîđ˙äî÷íî, íî ňŕę, ÷ňî â öĺëîě íŕ ýęđŕíĺ ďîëó÷ŕĺňń˙ äîâîëüíî đĺçęîĺ čçîáđŕćĺíčĺ ůĺëč äčŕôđŕăěű.
Îäíŕęî ĺńëč íŕ ďóňč «α-÷ŕńňčö ďîńňŕâčňü ěĺňŕëëč÷ĺńęóţ ôîëüăó, ňî âěĺńňî đĺçęîăî čçîáđŕćĺíč˙ ůĺëč íŕ, ýęđŕíĺ âîçíčęŕĺň đŕçěűňŕ˙ ďîëîńŕ. Ýňŕ ďîëîńŕ ëčřü íĺěíîăî řčđĺ čçîáđŕćĺíč˙ ůĺëč, ďîëó÷ĺííîăî â ďĺđâîě ńëó÷ŕĺ: α-÷ŕńňčöű îňęëîí˙ëčńü îň ďđ˙ěîăî ďóňč â ńđĺäíĺě âńĺăî íŕ 2 ăđŕäóńŕ. Îäíŕęî íĺńëîćíűé đŕń÷ĺň ďîęŕçŕë: ÷ňîáű îáú˙ńíčňü äŕćĺ ňŕęčĺ íĺáîëüřčĺ îňęëîíĺíč˙, íóćíî äîďóńňčňü, ÷ňî â ŕňîěŕő ôîëüăč ěîăóň âîçíčęŕňü îăđîěíűĺ ýëĺęňđč÷ĺńęčĺ ďîë˙ íŕďđ˙ćĺííîńňüţ ńâűřĺ 200 ňűń. â/ńě.
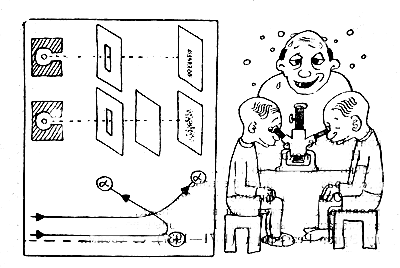
Ôîëüăŕ íŕ ďóňč ďîňîęŕ ÷ŕńňčö
 ďîëîćčňĺëüíîě řŕđĺ ŕňîěŕ Ňîěńîíŕ ňŕęčő íŕďđ˙ćĺííîńňĺé áűňü íĺ ěîćĺň. Ńňîëęíîâĺíč˙ ń ýëĺęňđîíŕěč ňŕęćĺ íĺ â ń÷ĺň: âĺäü ďî ńđŕâíĺíčţ ń íčěč «α-÷ŕńňčöŕ, ëĺň˙ůŕ˙ ńî ńęîđîńňüţ 20 ęě/ńĺę, âńĺ đŕâíî ÷ňî ďóřĺ÷íîĺ ˙äđî đ˙äîě ń ăîđîřčíîé. Č âńĺ ćĺ ďóňč «α-÷ŕńňčö čńęđčâë˙ëčńü.  ďîčńęŕő đŕçăŕäęč Ěŕđńäĺí ďđĺäëîćčë ďđîâĺđčňü: ŕ íĺ ěîăóň ëč «α-÷ŕńňčöű îňđŕćŕňüń˙ îň ôîëüăč íŕçŕä? Ń ňî÷ęč çđĺíč˙ ěîäĺëč Ňîěńîíŕ, ďđĺäëîćĺíčĺ ńîâĺđřĺííî áĺńńěűńëĺííîĺ: ďóřĺ÷íîĺ ˙äđî íĺ ěîćĺň îňđŕçčňüń˙ îň ăîđîřčíű. Đĺçóëüňŕň áűë íĺîćčäŕííűě, íî âďîëíĺ óáĺäčňĺëüíűě, őîň˙ ďîâĺđčňü â íĺăî áűëî ňđóäíî: «α-÷ŕńňčöű îňđŕćŕëčńü îň ôîëüăč.
Ďđîřëî äâŕ ăîäŕ. Çŕ ýňî âđĺě˙ Ăĺéăĺđ č Ěŕđńäĺí ńîń÷čňŕëč áîëĺĺ ěčëëčîíŕ ńöčíňčëë˙öčé č äîęŕçŕëč, ÷ňî îňđŕćŕĺňń˙ íŕçŕä ďđčěĺđíî îäíŕ «α-÷ŕńňčöŕ čç 8 ňűń˙÷.
Ňîëüęî ňĺďĺđü, 7 ěŕđňŕ 1911 ăîäŕ, Ěŕí÷ĺńňĺđńęîĺ ôčëîńîôńęîĺ îáůĺńňâî. — ňî ńŕěîĺ, ďđĺçčäĺíňîě ęîňîđîăî áűë ęîăäŕ-ňî Äćîí Äŕëüňîí, — óńëűřŕëî äîęëŕä Đĺçĺđôîđäŕ «Đŕńńĺ˙íčĺ α- č β-ëó÷ĺé č ńňđîĺíčĺ ŕňîěŕ».  ňîň äĺíü ńëóřŕňĺëč óçíŕëč, ÷ňî ŕňîě ďîäîáĺí ńîëíĺ÷íîé ńčńňĺěĺ: îí ńîńňîčň čç ˙äđŕ č ýëĺęňđîíîâ, ęîňîđűĺ âđŕůŕţňń˙ âîęđóă íĺăî íŕ đŕńńňî˙íč˙ő ≈ 10-8 ńě. Đŕçěĺđű ˙äđŕ î÷ĺíü ěŕëű — âńĺăî 10-13—10-12 ńě, íî â íĺě çŕęëţ÷ĺíŕ ďđŕęňč÷ĺńęč âń˙ ěŕńńŕ ŕňîěŕ. Çŕđ˙ä ˙äđŕ ďîëîćčňĺëĺí č ďî âĺëč÷číĺ đŕâĺí ďđčěĺđíî ďîëîâčíĺ ŕňîěíîăî âĺńŕ ýëĺěĺíňŕ. Ńđŕâíĺíčĺ ń ńîëíĺ÷íîé ńčńňĺěîé íĺ ńëó÷ŕéíî: äčŕěĺňđ ńîëíöŕ (1,4 • 106 ęě) ďđčěĺđíî âî ńňîëüęî ćĺ đŕç ěĺíüřĺ đŕçěĺđîâ ńîëíĺ÷íîé ńčńňĺěű (6 • 109 ęě), âî ńęîëüęî äčŕěĺňđű ˙äĺđ (≈ 10-12 ńě), ěĺíüřĺ đŕçěĺđîâ ŕňîěŕ (≈ 10-8 ńě).
Ěű íŕńňîëüęî ďđčâűęëč ę íîâűě ďîí˙ňč˙ě, ÷ňî, îáú˙ńí˙˙ ýëĺęňđîíčęó, ńńűëŕĺěń˙ íŕ ňĺëĺâčçîđ, ŕ đŕńńęŕçűâŕ˙ î ěĺőŕíčęĺ, ďđčâîäčě â ďđčěĺđ ďŕđîâîç. Ďîýňîěó ńĺé÷ŕń íŕě ňđóäíî ďîí˙ňü ňîăäŕříĺĺ íĺäîóěĺíčĺ ëţäĺé, ďî ńčëĺ óěŕ ďîäîáíűő Đĺçĺđôîđäó. Äĺéńňâčňĺëüíî, äë˙ íŕń ńĺé÷ŕń âńĺ ňŕę ďđîçđŕ÷íî: ďđîńňî «α-÷ŕńňčöŕ îňđŕćŕĺňń˙ îň ˙äĺđ ŕňîěîâ. Č ę ýňîé ęŕđňčíĺ ěű ďđčâűęŕĺě ń äĺňńňâŕ. Íî ÷ňîáű íŕđčńîâŕňü ĺĺ â ďĺđâűé đŕç, íĺîáőîäčěŕ áűëŕ âűäŕţůŕ˙ń˙ íŕó÷íŕ˙ ńěĺëîńňü, îńíîâŕííŕ˙ íŕ çíŕíčč, äîáűňîě áîëüřčě ňđóäîě. Ďđĺćäĺ ÷ĺě ýňŕ ęŕđňčíŕ ńňŕëŕ čçâĺńňíŕ ęŕćäîěó, ďđčřëîńü íĺ ňîëüęî ńîń÷čňŕňü ńâűřĺ ěčëëčîíŕ ńöčíňčëë˙öčé: íóćíî áűëî (ęŕę âńďîěčíŕë â ęîíöĺ ćčçíč Ăĺéăĺđ) «...ďđĺîäîëĺňü ňŕęčĺ ňđóäíîńňč, ńěűńë ęîňîđűő ěű ńĺé÷ŕń äŕćĺ ďîí˙ňü íĺ â ńîńňî˙íčč»; íóćíî áűëî ńíŕ÷ŕëŕ â ňĺ÷ĺíčĺ äĺń˙ňč (!) ëĺň äîęŕçűâŕňü, ÷ňî «α-÷ŕńňčöű — íĺ ÷ňî číîĺ, ęŕę ŕňîěű ăĺëč˙, ďîňĺđ˙âřčĺ äâŕ ýëĺęňđîíŕ, Äîęŕçŕňĺëüńňâî îęŕçŕëîńü íĺďđîńňűě, č Řâĺäńęŕ˙ ŕęŕäĺěč˙ íŕóę őîđîřî ďîíčěŕëŕ ýňî, ęîăäŕ â 1908 ăîäó ďđčńóäčëŕ Đĺçĺđôîđäó Íîáĺëĺâńęóţ ďđĺěčţ çŕ čńńëĺäîâŕíč˙ ďî őčěčč đŕäčîŕęňčâíűő âĺůĺńňâ, â đĺçóëüňŕňĺ đŕńďŕäŕ ęîňîđűő îáđŕçóţňń˙ α-÷ŕńňčöű. Îáî âńĺě ýňîě ďîńňĺďĺííî çŕáűëč: đĺçóëüňŕň áűë âŕćíĺĺ č ďđîůĺ, ÷ĺě ďóňü, ę íĺěó ďđčâĺäřčé.
Čńńëĺäîâŕíčĺ Đĺçĺđôîđäŕ
Ńîîáůĺíčĺ Đĺçĺđôîđäŕ ôčçčęč ďđčí˙ëč ńäĺđćŕííî. Ńŕě îí â ňĺ÷ĺíčĺ äâóő ëĺň ňŕęćĺ íĺ î÷ĺíü ńčëüíî íŕńňŕčâŕë íŕ ńâîĺé ěîäĺëč, őîň˙ č âĺđčë â áĺçîřčáî÷íîńňü îďűňîâ, ęîňîđűĺ ę íĺé ďđčâĺëč. Ďđč÷číŕ áűëŕ âńĺ ňŕ ćĺ: ĺńëč âĺđčňü ýëĺęňđîäčíŕěčęĺ, ňŕęŕ˙ ńčńňĺěŕ ńóůĺńňâîâŕňü íĺ ěîćĺň, ďîńęîëüęó ďî ĺĺ çŕęîíŕě âđŕůŕţůčéń˙ ýëĺęňđîí íĺčçáĺćíî č î÷ĺíü áűńňđî óďŕäĺň íŕ ˙äđî. Ďđčőîäčëîńü âűáčđŕňü: ëčáî ýëĺęňđîäčíŕěčęŕ, ëčáî ďëŕíĺňŕđíűé ŕňîě. Ôčçčęč ěîë÷ŕ âűáđŕëč ďĺđâîĺ. Ěîë÷ŕ ďîňîěó, ÷ňî îďűňű Đĺçĺđôîđäŕ íĺëüç˙ áűëî íč çŕáűňü, íč îďđîâĺđăíóňü. Ôčçčęŕ ŕňîěŕ çŕřëŕ â ňóďčę. Č ÷ňîáű âűéňč čç íĺăî, íóćĺí áűë Íčëüń Áîđ.
|
ĎÎČŃĘ:
|
© NPLIT.RU, 2001-2021
Ďđč čńďîëüçîâŕíčč ěŕňĺđčŕëîâ ńŕéňŕ ŕęňčâíŕ˙ ńńűëęŕ îá˙çŕňĺëüíŕ:
http://nplit.ru/ 'Áčáëčîňĺęŕ ţíîăî čńńëĺäîâŕňĺë˙'
Ďđč čńďîëüçîâŕíčč ěŕňĺđčŕëîâ ńŕéňŕ ŕęňčâíŕ˙ ńńűëęŕ îá˙çŕňĺëüíŕ:
http://nplit.ru/ 'Áčáëčîňĺęŕ ţíîăî čńńëĺäîâŕňĺë˙'