
Глава пятая. Молекулярная биология и вирусы
Нам казалось логичным и оправданным из стратегических, что ли, соображений самые трудные (и потому, возможно, достаточно скучные) главы - о методах вирусологии поместить вначале. Ведь как человек обычно поступает, беря в руки незнакомую книгу и раздумывая: купить или не покупать, читать или обойтись без содержащейся в ней информации? Пролистывает, отмечая, есть ли иллюстрации, много ли коротких строчек, абзацев, как называются главы. Интуитивно эта поверхностная характеристика оценивается, и на этом основании принимается то или иное решение.
Так вот экспериментально установлено: расположение привлекающих читателя параметров во второй части книги, ближе к концу, способствует покупке. Ну, и наконец, такое соображение. В научных статьях, монографиях, диссертациях не случайно раздел "Материалы и методы" помещают раньше основной части работы, чтобы понять и оценить результаты, надо знать (и быть уверенным в их достоверности), как эти результаты удалось получить.
Короче, после этого небольшого извинения за трудность и малоинтересность, начинаем разговор о молекулярной биологии вирусов и методах, которыми эта наука оперирует... Впрочем, может быть, мы и не правы: ведь молекулярная биология - это не только методы, но еще и в немалой степени философия, так что, если в этой главе не будет споров, то без размышлений не обойтись.
Строго говоря, молекулярная биология - самостоятельная наука, касающаяся в равной степени и генетики, и физиологии, и органической химии, и вирусологии... Проще, казалось бы, перечислить, каких разделов биологии и смежных с ней дисциплин естествознания она не касается, чем назвать те, в которых ее интересы непосредственно затронуты. Так вот, дисциплин, которых она бы не касалась, нет. И ничего странного в этом также нет: поскольку любой субъект, как и любой объект, состоит из молекул, молекулярной биологии до всего есть дело.
Молекулярная биология появилась в начале 50-х годов нашего столетия, и уже через несколько лет было провозглашено, что рождение этой дисциплины является второй революцией в естествознании XX века. Почему второй? Потому что первой, не соблюдая субординацию (привычнее идти от более крупного к более мелкому), стала революция, связанная с физикой атомной, физикой элементарных частиц, имевшая место, как известно, в самом начале века.
Вероятно, вопреки кажущемуся парадоксу в таком порядке есть своя логика. Конечно, молекулы крупнее атомов, но изучать их из-за этого вовсе не проще: ведь они гораздо сложнее устроены, в них тысячи и тысячи "и" Берталанфи, и каждое тем или иным образом влияет на свойства, причины и следствия. Кроме того, молекулярная биология не могла появиться на голом месте, ибо она должна была воспользоваться техникой, понятиями и представлениями первой революции. Наконец, нужны были и специалисты, которые бы не только сделали революцию, но и поняли, что же они сотворили.
Итак, это произошло в 50-е... А в 70-е, по словам академика В. А. Энгельгардта, утверждение, что молекулярная биология стала одной из ведущих областей современного естествознания и вывела науку о живом в один ряд с важнейшими разделами точных наук - физики, химии, космологии - стало настолько очевидным, что есть опасение превращения его в некий трюизм, истину, которая навязла в зубах.
Молекулярная биология - не просто еще одна из новых научных дисциплин, какие сегодня постоянна рождаются в любой отрасли знаний. Более того, между рождением этих дисциплин и появлением понятия молекулярная биология нет ничего общего. Потому что все новые дисциплины - уход в частности, отторжение от материнского древа породившей ее науки. К тому же каждая новая дисциплина становится самостоятельной, как правило, лишь когда учеными осознается отличительность объекта исследований и появляются собственные, специфические методы для них. Так произошло, в частности, и с самой вирусологией: Ивановский доказал существование особых, специфических "объектов исследования" - вирусов и использовал для их изучения новый, опять-таки специфический метод - фильтрацию (или как тогда говорили - ультрафильтрацию).
Молекулярная биология, наоборот, родилась на стыке практически всех естественнонаучных дисциплин, изучающих проблему живого, проблему жизни как естественный и органический синтез физики, органической химии, генетики, цитологии и целого ряда других наук, включая математический анализ. Рожденная в итоге такого гигантского творческого синтеза молекулярная биология смогла "обратить свое внимание" практически на любой биологический объект. Так появилась молекулярная биология клетки, молекулярная биология бактерий, молекулярная биология вирусов...
Какими же основными методами пользуются в своих исследованиях специалисты по молекулярной биологии вирусов? Прежде всего практически всеми, которые известны для вирусологии вообще. Ведь перед тем как приступить к молекулярно-биологическим исследованиям, вирус надо накопить, выделить, идентифицировать. Все это делается с помощью собственно вирусологических методов исследования, о которых мы говорили выше. Затем вирус надо очистить от балластных примесей, ибо в каком бы субстрате мы его ни накапливали, на одну вирусную приходится миллионы частиц, никак с ней не связанных, а относящихся к телу хозяина, где этот вирус репродуцировался.
Способов очистки много, в том числе очень широко применяется и такой, чисто вирусологический, как "адсорбция - элюция". Несмотря на внешнюю примитивность (в наш век сложнейшей техники для этого метода нужна лишь ручная центрифужка), он обладает высокой эффективностью и позволяет не только чистить, но и концентрировать вирусы. Суть его состоит в том, что многие вирусы обладают горячей, хотя и кратковременной, "любовью" к эритроцитам некоторых животных или человека. И если в содержащую вирус жидкость влить подходящие эритроциты, все наличные вирионы быстро вступят с ними в контакт. Эритроциты очень крупные (по сравнению с бактериями, белками, обломками клеток) образования, они оседают на дно даже при невысоких скоростях вращения. Слив надосадочную жидкость и добавив к эритроцитам свежий физиологический раствор, мы очень легко получим достаточно чистую взвесь вируса, так как через час-два "любовь" кончается и вирусы с поверхности эритроцитов отскакивают (элюируют).
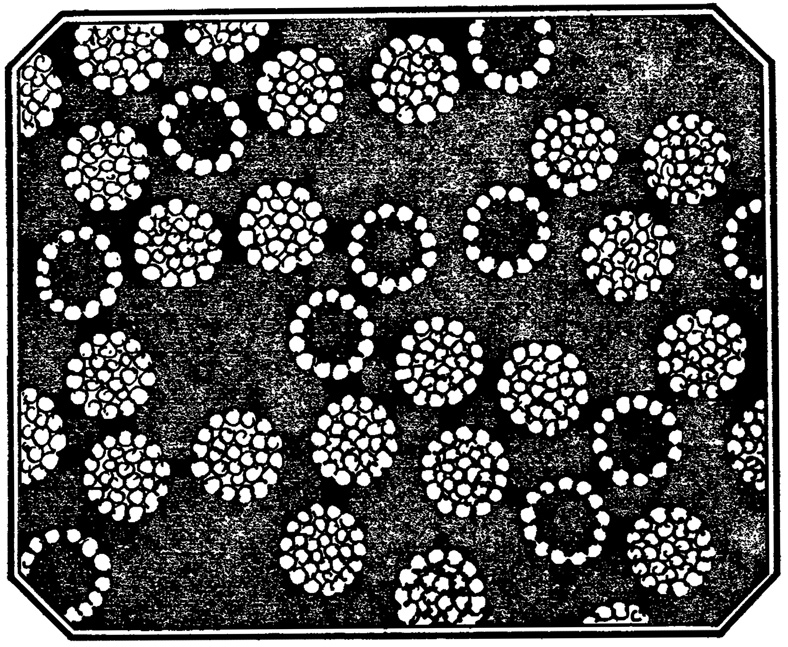
Рис. 4
Итак, первичная, грубая, но необходимая для последующей работы очистка и концентрация содержащего вирус материала проведена. Но это только начало пути, по которому можно прийти к высоко очищенной взвеси вирионов, при электронной микроскопии она выглядит так, как показано на рисунке.
Препарат такой чистоты, как на рисунке, путем адсорбции - элюции с эритроцитов не получишь. Для этого нужны другие методики, и главные из них - ультрацентрифугирование и хроматография.
Приставка ультра (от латинского сверх, за пределом) встречается в нашей речи, да и в этой книге достаточно часто. Ультрамодная одежда, ультрасовременная техника... Во всех этих случаях, собственно, как и в термине ультрацентрифугирование, больше абстрактного, нежели конкретного содержания. А если говорить именно конкретно, о вирусах и молекулярной биологии, надо понимать, что метод заключается все же в центрифугировании, то есть во вращении пробы вокруг какой-то оси, но со скоростью значительно превышающей средние, обычные показатели.
Для чего нужно вращать пробу? При вращении возникают две силы: центростремительная и центробежная. В принципе они равны, но действуют на разные объекты: первая - на связь, тело удерживающую, вторая - непосредственно на тело. Следовательно, если изготовить связь достаточно прочную, можно получить центробежную практически в чистом виде. А это очень важно, ибо в таком случае величина силы может быть огромной.
Формула центробежной силы mv2/R, где m - масса тела, v - его скорость, R - радиус кривизны траектории. Уже при беглом взгляде на формулу понятно, благодаря чему происходят очистка и концентрация вируса. Ведь если раскручивать смесь, состоящую из материальных частиц разной массы, то более тяжелые приобретут большую центробежную силу и за одинаковое время успеют убежать от центра дальше тех, которые полегче.
При центрифугировании (любом, и ультра и не ультра) вируссодержащая жидкость расслаивается. Что-то выпадает в осадок, что-то оказывается около дна, что-то в середине центрифужной пробирки или стакана. Правда, при замедлении вращения после выключения центрифуги и последующих манипуляциях эти слои могут снова в какой-то степени перемешаться из-за броуновского (теплового) движения. Чтобы этого не произошло или, по крайней мере, чтобы смешалось как можно меньше, ученые идут на дополнительные меры - охлаждают смесь и помещают вируссодержащий материал в какие-либо вязкие растворы различной концентрации. Растворы имеют разную плотность (градиент плотности), и тоже располагаются слоями, в один из которых и "загоняют" или ловят вирус. Это очень красивое зрелище - зона опалесценции, видимая даже невооруженным глазом, из- за того что многие миллиарды вирионов собраны в ограниченном объеме.
Чтобы больше не возвращаться к ультрацентрифугированию, скажем еще, что этот же метод используется и для изучения внутренней структуры вирионов. Помещая совсем уже очищенный вирус в жидкость с разным градиентом плотности и раскручивая до ультраскоростей, можно разорвать вирион на части и сконцентрировать обломки в том или ином слое.
Ультрацентрифуга - очень сложная машина, требующая особых условий установки, охлаждения трущихся деталей и т. д. И хотя в ряде случаев без таких аппаратов не обойтись, очень часто оказывается возможным чистить и концентрировать вирусы с помощью бесшумного, безопасного и малоэнергоемкого метода хроматографии.
Хроматография основана совсем на другом принципе. Вирионы избирательно сорбируются, но не на эритроцитах, а на особых пористых веществах, а потом элюируют оттуда в солевые растворы. Таким путем получена, например, сверхчистая гриппозная вакцина учеными Ленинградского научно-исследовательского института микробиологии и эпидемиологии имени Л. Пастера и биофизиками Ленинградского политехнического института имени М. И. Калинина. В этом случае для хроматографической очистки используют так называемое широкопористое стекло.
Нет предела совершенству! Можно и так и эдак чистить вирус, доводя эту процедуру до получения взвеси одних только вирионов, практически без всяких примесей (кстати, советская хроматографическая вакцина относится к категории именно таких препаратов, недаром ее называют сверхчистой!), но это всего лишь начало молекулярной биологии вирусов. Вирусология начинается с накопления вирусной биомассы, молекулярная вирусология - с ее очистки. Впрочем, для такого дела, как получение вакцин, эта процедура является финальной - недаром же говорят: "центрифужная вакцина", "хроматографическая вакцина"...
Если очистка и концентрация вирусной взвеси - начало, то что же является продолжением? Это, конечно, зависит от цели работы, но так или иначе сводится к исследованию отдельных компонентов вириона, главным образом белков и нуклеиновых кислот.
Чтобы выделить какой-то компонент вириона, его надо разорвать, разрезать, то есть каким-то образом нарушить целостность и обеспечить возможность разным частям его путешествовать по самостоятельным маршрутам. Для этого используют несколько различных приемов, но суть их одна: дезинтегрировать (разрушить) вирусную частицу, разделить белковые компоненты и нуклеиновую кислоту и порознь изучить их. Часто прибегают к электрофорезу в своеобразном студнеобразном веществе, так называемом полиакриламидном геле (ПААГ). Электрофорез - разделение частиц исследуемого вещества по скорости их продвижения в этом геле при пропускании электрического тока. В зависимости от массы и заряда разные частички вещества пройдут в геле разное расстояние. А если вещество (белок или нуклеиновую кислоту) покрасить или пометить радиоактивными изотопами, то в полоске геля отчетливо можно будет обнаружить полосы, представляющие скопления однотипных молекул. Так выявляются отдельные полипептиды (кирпичики индивидуальных белков) или фрагменты однотипных молекул нуклеиновой кислоты. Так, "портретом" РНК вируса гриппа является электрофореграмма. Отчетливо видны 8 полос, соответствующих 8 фрагментам (генам) этого возбудителя. Каждый ген кодирует определенный белок, поэтому при электрофорезе в ПААГ белков можно отчетливо видеть 8 различных полипептидов, пробежавших в электрическом поле разное расстояние: самые крупные (тяжелые) белки, так называемые полимеразные (мы подробно поговорим об их роли дальше) прошли самое малое расстояние, самые легкие, так называемые неструктурные - самое большое.
"Портреты" белков и нуклеиновых кислот вирусов, полученные описанным методом, дают самое общее представление об индивидуальности вирусов, а очень часто нужны более точные и подробные сведения. Поэтому каждый полипептид исследуется еще и по пептидному составу (пептид - цепочка из нескольких аминокислот, полипептид - совокупность отдельных пептидов), а нуклеиновая кислота (РНК и ДНК) по олигонуклеотидному. Элементарный "кирпичик" нуклеиновой кислоты - мононуклеотид, несколько мононуклеотидов составляют олигонуклеотид, который в совокупности и есть полинуклеотид (нуклеиновая кислота). Подробнее об этом в следующей главе.
Методы пептидного и олигонуклеотидного анализа (так называемого картирования) дают своеобразные картины, напоминающие отпечатки пальцев, где каждое пятно соответствует какому-то конкретному пептиду или олигонуклеотиду. Сравнивая эти отпечатки между собой, можно сделать вывод о сходстве или различии соответствующих структур тех или иных вирусов. Такой же вывод можно сделать, если гибридизировать (смешивать при определенных условиях) нуклеиновые кислоты разных вирусов, а потом подвергать эти комплексы электрофорезу. Если участки гибридизуемых нуклеиновых кислот полностью гомологичны друг другу, то подвижность такого комплекса (его называют дуплексом) будет иной, чем при частичной гомологии.
Такой метод носит название молекулярной гибридизации нуклеиновых кислот. Его результаты могут выявиться и при сравнительном электрофорезе разных образцов, и другими методами, например, в "пятне" - так называемая ДОТ (точечная гибридизация). В этом случае одна нуклеиновая кислота (известная по своей структуре) используется как своеобразная удочка (молекулярный зонд) для ловли гомологичных ей участков вирусной нуклеиновой кислоты в тех или иных материалах. Ответ здесь, как правило, получается по принципу "да - нет", но как важен он и в такой форме применительно, скажем, к целям диагностики, точнее - молекулярной диагностики, вирусных инфекций!
Здесь мы можем сделать некоторые обобщения. Строго говоря, все виды исследования вирусов, с которыми мы познакомились, четко укладываются всего в... 4 группы. Во-первых, это исследование вирусов (или их компонентов) как таковых (по-латыни - per se, то есть в чистом виде). Это касается электронной микроскопии вирионов, изучения их биофизических свойств (например, плотности, электрического заряда и т. д.), а также всех свойств вирусных компонентов - белков, нуклеиновых кислот и др.
Во-вторых, это исследование вирусов с помощью (точнее - посредством) клеток. Сюда относятся все виды накопления вирусов во всех системах живых клеток, а также все виды индикации вирусов по их цитопатогенному действию, реакции гемагглютинации, гемадсорбции и т. д.
В-третьих, это исследования вирусов с помощью (или опять-таки точнее - посредством) антител - идентификация. Мы достаточно подробно говорили о разных видах реакций вирус (антиген) - антитело, не будем повторяться.
Наконец, четвертая группа методов изучения вирусов связана с молекулярной гибридизацией вирусных нуклеиновых кислот. Об этом мы сказали только что, но...
Здесь надо сделать очень важное отступление, точнее, коснуться совершенно нового вопроса и поговорить о генной инженерии и ее роли в вирусологии. Именно она дала вирусологии в последние годы принципиально новые возможности: и накапливать компоненты вируса при отсутствии чувствительных клеток, и получать молекулярные зонды, способные с огромной чувствительностью обнаруживать гомологичные нуклеиновые кислоты в разных субстратах, и получать самую полную информацию о белках и нуклеиновых кислотах вирусов, об их первичной структуре, то есть о последовательности нуклеотидов в гене, и о последовательности аминокислот в белковой молекуле.
Что же такое генная инженерия?
Генная инженерия - раздел молекулярной биологии, впрочем, можно говорить о том, что это одновременно и ее порождение и ее дальнейшее развитие. Вспомним, что молекулярной биологией можно назвать науку, изучающую структуру и функции важнейших биополимеров - белков и нуклеиновых кислот. В рамках этой науки было сделано важнейшее открытие, о котором мы будем далее подробно говорить: открытие особого фермента, способного синтезировать ДНК на матрице РНК. Фермент этот - обратная транскриптаза (или ревертаза) позволяет вести ферментативный синтез генов вне клеток (in vitro). Произошло это в 70-е годы.
В те же 70-е годы произошло и другое важное событие: были открыты ферменты, способные разрезать и сшивать молекулы ДНК: рестриктазы (ферменты разрезания) и лигазы (ферменты сшивания). Эти два открытия идеально дополнили друг друга: недаром 70-е годы называются эпохой "Двух Р" ("ревертаза+рестриктаза"). За открытие ревертазы Г. Темин и Д. Балтимор получили Нобелевскую премию в 1975 году, за открытие ферментов рестрикции А. Арбор, Г. Натане и К. Смит были вознаграждены таким же образом в 1979 году. Почему же эти два открытия так тесно связаны?
Повторим: ревертаза позволяет синтезировать ген in vitro, рестриктазы и лигазы позволяют этот ген встроить практически в любую другую ДНК, скажем, бактериальной клетки, где он будет реплицироваться вместе с хозяйской ДНК и таким образом размножаться. Итак, если молекулярная биология привела к искусственному синтезу генов, то размножением этих генов занялась целая новая отрасль знаний - генная инженерия.
Определим новую науку несколько строже. Это специальная дисциплина, объект изучения и приложения которой - ген (ДНК), как естественный, так и искусственно полученный с помощью ревертазы. Генная инженерия включает в себя методы, позволяющие встраивать эти гены in vitro (с помощью названных выше ферментов - рестриктаз и лигаз) в ДНК бактерий, вирусов и клеток высших животных. Затем вводить полученные при этом рекомбинантные (гибридные) молекулы в соответствующие (так называемые пермиссивные, то есть чувствительные) клетки, добиваясь "приживления", репликации (размножения) гибридных ДНК как своих собственных, и, наконец, экспрессии, то есть выражения той информации, которая в этих генах содержится.
Генная инженерия - основа современной биотехнологии, а последняя - принципиально новое направление технологии, отличающееся высокими потенциальными возможностями благодаря использованию в промышленных масштабах процессов биокатализа, биоконверсии и биотрансформации энергии и вещества. Возможности биотехнологии простираются от получения новых лекарственных препаратов до новых источников энергии (производство этанола, бутанола, водорода и метана), от охраны окружающей среды (микробиологическая очистка сточных вод и газовых выбросов) до добычи полезных ископаемых методами биосорбции, от пищевого и кормового белка до ферментов промышленного назначения, от новой технологии сельскохозяйственного производства, включая высокопродуктивные сорта культурных растений, сконструированных генно-инженерными способами и оригинальных приемов агротехники, основанных на биологических способах борьбы с сорняками, до новых компьютеров и голографических матриц, сконструированных с применением принципов биологических систем и биоматериалов. Все эти приемы и методы в той или иной степени используются сегодня в вирусологии, дополняя арсеналы собственно вирусологических способов исследования.
|
ПОИСК:
|
© NPLIT.RU, 2001-2021
При использовании материалов сайта активная ссылка обязательна:
http://nplit.ru/ 'Библиотека юного исследователя'
При использовании материалов сайта активная ссылка обязательна:
http://nplit.ru/ 'Библиотека юного исследователя'