
В крови плавают десятки тысяч различных антител, но они имеют общий план стоения
— Как устроены молекулы антител? Это, наверное, белки, которые циркулируют в крови.
— Да, это самые крупные белковые молекулы кровяной сыворотки — гамма-глобулины. Поскольку все гамма-глобулины — антитела, их теперь называют иммуноглобулинами.
— Сколько же разных иммуноглобулинов плавает в крови?
— Много. По приблизительным подсчетам, около десяти тысяч. Около одного процента массы крови приходится на иммуноглобулины. Иначе говоря, в литре крови 10 граммов антител.
— Сколько же это молекул?
— Очень много. Цифра астрономическая. Что-то вроде 5Х1020 (500 000 000 000 000 000 000), и каждая из них может соединиться с каким-то чужеродным веществом и обезвредить его.
Расшифровать устройство молекулы иммуноглобулина удалось благодаря работам двух исследователей — Роднея Портера в Оксфорде и Джералда Эдельмана в Нью-Йорке. Первые результаты были опубликованы в 1959 году. К 1965 году в общих чертах структура молекулы была расшифрована. К 1970-му иммунологи знали не только план строения, но и последовательность укладки «кирпичей» (аминокислот, из которых построена любая белковая молекула). В 1972 году Портер и Эдельман были удостоены Нобелевской премии.

Работа в поте лица
Примерный ход событий таков. В 1958 году Портер обработал выделенный из крови чистый иммуноглобулин папаином. Его получают из растений. Папаин относится к ферментам, разрушающим белки. Он способен разрезать белковые молекулы поперек.
В это же самое время на другом берегу Атлантического океана, как говорят в науке, «одновременно и независимо» Эдельман обработал выделенные из крови молекулы иммуноглобулинов 6-меркаптоэтанолом. Этот химический реагент обладает способностью разрезать молекулы белков вдоль. (Папаин пилит белковые стволы на дрова, а 6-меркаптоэтанол — на доски.)
Здесь следует немного отвлечься от антител, чтобы вспомнить, как вообще построены белки, что лежит в их основе.
Основой строения всех белков служат пептидные цепи. Белок может быть составлен из нескольких цепей, расположенных последовательно или параллельно друг другу. Каждая цепь, как из звеньев, образована из аминокислот. Вот, например, кусочек пептидной цепи инсулина — одного из хорошо изученных белков, при недостатке которого развивается тяжелая болезнь диабет: цистеин—аланин—серин—валин—цистеин. Полипептидные цепи, составленные из разных сочетаний 20 аминокислот, образуют все многообразие белков на нашей планете.
Аминокислоты соединены в цепи пептидов через атомы углерода и азота. Эти связи носят название пептидных. Именно их разрывает папаин. Конечно, не все сразу. В первую очередь в наиболее доступных участках белковой молекулы.
Если пептидные цепи, составляющие молекулу белка, расположены в виде двух нитей параллельно друг другу, то они соединяются между собой через два атома серы. Эти связи называются дисульфидными. Их разрушает 6-меркаптоэтанол. В результате этого белковая молекула, если она составлена из параллельных пептидных цепей, разрезается вдоль.
Итак, Портер рассек молекулу антитела поперек, а Эдельман вдоль.
Молекулярный вес целой молекулы был чуть больше 150 тысяч. После поперечного разрезания возникли три фрагмента с молекулярным весом около 50 тысяч каждый. Портер получил три фрагмента примерно равной величины. Он обозначил их I, Пи III. Величина их была почти равна, но свойства...
Фрагменты I и II оказались тождественными друг другу. Каждый из них обладал главным качеством антитела — мог соединяться с антигеном, с той чужеродной субстанцией, против которой направлено данное антитело. Фрагмент III этим качеством не обладал.
Эдельман получил четыре фрагмента, вернее, четыре цепи, так как он разделил белковую молекулу на пептидные цепи. Две цепи, тождественные между собой, имели молекулярный вес примерно 25 тысяч. Он их назвал L-цепи (от слова light — легкий). Две другие, тоже тождественные между собой, имели вес 50 тысяч. Он их назвал Н-цепи (от слова haevy — тяжелый). (Следует заметить, если одна пептидная цепь в два раза тяжелее другой, это значит, что она в два раза длиннее.) Ни одна из этих цепей основным качеством антитела — способностью связывать антиген — не обладала. Однако если воссоединить вновь L-цепь и Н-цепь, то у образовавшейся структуры, представляющей половину молекулы, это качество восстанавливалось.
Вот так перед исследователями возникла задачка на сообразительность.
Дано: если разрезать молекулу поперек, возникает три части. Обозначим молекулярный вес в тысячах внизу символа, а антительную активность — звездочкой вверху символа. Получим формулу строения антитела: АТ150 = I50 * + II50 * + III50.
Если разрезать вдоль, возникает четыре части со своей формулой: АТ150 = 2L25 +2Н50 = (L25 + Н50) * + (L25 + Н50)*.
Требуется: определить пространственную структуру расположения пептидных цепей в молекуле и локализацию активных центров, то есть участков, определяющих главное качество — способность соединяться с антигеном.
Еще упрощаем задачу: из двух длинных и двух коротких цепочек сложить фигуру, которая бы при поперечном разрезе давала три равновеликих фрагмента. Два из них несут специфические антигенсвязывающие участки, составленные из длинной и короткой цепей.
Получится конструкция, похожая на заглавную букву «игрек» латинского шрифта Υ , что-то вроде нашей мальчишеской рогатки. Места, к которым привязывается резинка, и есть активные центры. Две стороны «рогатины» — это и есть портеровские фрагменты I и II. «Рукоятка» — фрагмент III. Папаин рассекает конструкцию на три фрагмента как раз в месте разветвления.
Две длинные цепи, располагаясь рядом друг с другом, формируют «рукоятку», а в месте разветвления расходятся, образуя внутренние стороны «рогатины». Короткие цепи примыкают к длинным после развилки, формируя наружные стороны «рогатины». Концы ее, состоящие из окончаний обоих типов цепей, определяют специфичность молекулы. В итоге каждое антитело имеет два активных центра. Как двумя руками связывает оно чужеродные антигенные частицы, делая их неактивными, нерастворимыми, неспособными оказывать вредное организму действие.
Такая конструкция построена не только на основе логических рассуждений. Она подтверждена специальными физико-химическими методами. Наконец, ее увидели в электронном микроскопе. Молекула антитела действительно выглядит так:
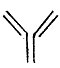
Малекула антитела
Некоторые молекулы антител соединяются своими «рукоятками» по две. Тогда они называются димерами. Они имеют, таким образом, сразу четыре активных центра для связывания антигена. Так ведут себя иммуноглобулины класса А. Другие молекулы объединяются по пять (пентамеры), образуя картину звезды с десятью активными центрами, смотрящими наружу. Это иммуноглобулины класса М. Но большинство антител относятся к обычному, мономерному («моно» — значит «один») типу. Их называют иммуноглобулинами класса Г.
К 1970 году структура антител была понята не только в общих чертах. Было выяснено, сколько аминокислот в каждой из четырех пептидных цепей.
Легкие цепи человеческих иммуноглобулинов оказались составленными из 214 аминокислот каждая, а тяжелые из 428. Молекула антитела наиболее распространенного класса Г сложена из 1284 аминокислот. Но не все они формируют каждый из двух активных центров молекулы. Специфические участки, которыми молекула распознает чуждый антиген и связывает его, образованы не более чем десятками аминокислот. Однако, чтобы построить их пространственно правильно, работают по 107 первых аминокислот каждой из четырех цепей. Они расположены на концах «рогатины». Участки цепей, составленные из них, называются вариабельными, потому что аминокислотная последовательность в этих участках в разных молекулах варьирует. У каждого антитела своя последовательность.
|
ПОИСК:
|
© NPLIT.RU, 2001-2021
При использовании материалов сайта активная ссылка обязательна:
http://nplit.ru/ 'Библиотека юного исследователя'
При использовании материалов сайта активная ссылка обязательна:
http://nplit.ru/ 'Библиотека юного исследователя'