
УРАВНЕНИЕ ШРЕДИНГЕРА
Предыдущие рассказы о квантовой механике почти убедили нас в том, что электрон в атоме не имеет определенного положения или хотя бы какой-нибудь орбиты, по которой он движется. Взамен этого мы пока что усвоили довольно туманную идею о том, что при движении в атоме электрон «расплывается».
Эту неопределенную идею Шредингеру удалось выразить весьма точно на однозначном языке формул. Уравнение Шредингера, как и всякий глубокий закон природы, нельзя вывести строго из более простых. Его можно только угадать. Шредингер так и сделал, и впоследствии признавался, что сам не вполне понимает, как это ему удалось. Но после того как уравнение угадано, надо еще научиться им пользоваться: надо знать, что означают все символы в уравнении и какие явления в атоме они отображают.
Уравнение Шредингера
[(d2 ψ)/(dx2) + 2m/ħ2][E - U(x)(x)]ψ = 0
мы уже приводили однажды и объясняли смысл входящих в него символов: ħ - постоянная Планка h, деленная на 2π m — масса электрона, Е — полная энергия электрона в атоме a U(х) — его потенциальная энергия, которая показывает, с какой силой притягивался бы электрон к ядру, если бы он был частицей и находился от него на расстоянии х. Но нам по-прежнему неясен смысл волновой функции пси (ψ). Чтобы ронять его, обратимся снова к аналогии с колеблющейся струной.

Уравнение Шредингера
Ее уравнение
[(d2U)/(dx2)] + [2π/λ]2U = 0
очень похоже на уравнение Шредингера. Несколько решений уравнения струны, функции U = Uk(x), изображено на рисунке. Это обычные, знакомые всем синусоиды, и смысл их очевиден: они изображают форму струны в какой-то момент времени, то есть моментальную фотографию процесса ее колебания. Форма колебаний струны зависит от числа узлов k — точек, остающихся неподвижными в процессе колебания. Поэтому существует бесконечно много решений U=Uk(x), которые различаются между собой числом узлов k.
Теперь взгляните на рисунок, где рядом с синусоидами струны Uk((x) изображены решения ψ = ψn(x) уравнения Шредингера для атома водорода. Они очень похожи. И если даже никаких реальных колебаний, подобных движениям струны, в атоме не происходит, то аналогия не становится от этого менее полезной.
Отмеченная аналогия позволяет пронумеровать решения ψn(x) целым числом n точно так же, как решения Uk(x) нумеруются целым числом к. Более того, оказалось, что целое число n — это и есть то самое непонятное квантовое число, которым Бор нумеровал орбиты электрона в атоме. Теперь оно потеряло свой мистический оттеннок: n — не что иное, как число узлов волновой функции, увеличенное на единицу (n = k + l).
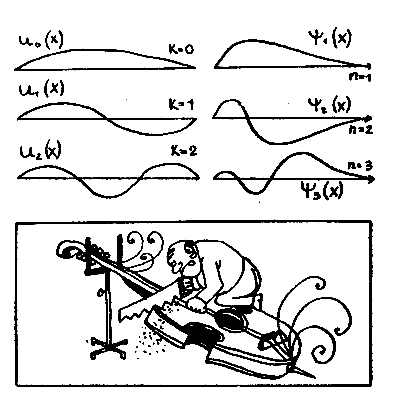
Струны
Первый постулат Бора неким «усилием воли» предписывал электронам двигаться только по тем орбитам в атоме, которые удовлетворяют квантовому условию:
m v; к = n(h/2π)
Это был плодотворный, но неестественный для физики принцип, и потому он вызвал у современников сложную смесь восхищения и недовольства. Требование Шредингера значительно естественнее: как бы хитро ни двигался электрон в атоме, он должен все-таки находиться внутри атома. Поэтому ψ-функция, которая это движение «представляет», независимо от своей природы должна быть сосредоточена вблизи ядра. Это единственное граничное условие позволило вывести из уравнения Шредингера все: условия квантования Бора, энергию электрона на стационарных орбитах, смысл квантовых чисел.
В свое время эти следствия теории Шредингера покорили многих своей простотой. В уравнение Шредингера поверили и стали выяснять последнее: что представляет собой сама функция ψ.
И если функция Uk(x) изображает форму колеблющейся струны, то что изображает ψ?
Смотрите подробности морозильные лари здесь.
|
ПОИСК:
|
При использовании материалов сайта активная ссылка обязательна:
http://nplit.ru/ 'Библиотека юного исследователя'